ANMAT prohíbe un tornillo traumatológico SPIN® 2.0 sin registro: los riesgos directos
- curecompass
- 10 marzo, 2026
- Gobierno, Medicina, Salud
- ANMAT, cirugía traumatológica, fijación de fragmentos óseos, Portada, Registro Nacional de Productores y Productos de Tecnología Médica, SPIN®, tornillos traumatológicos, traumatología
- 0 Comments
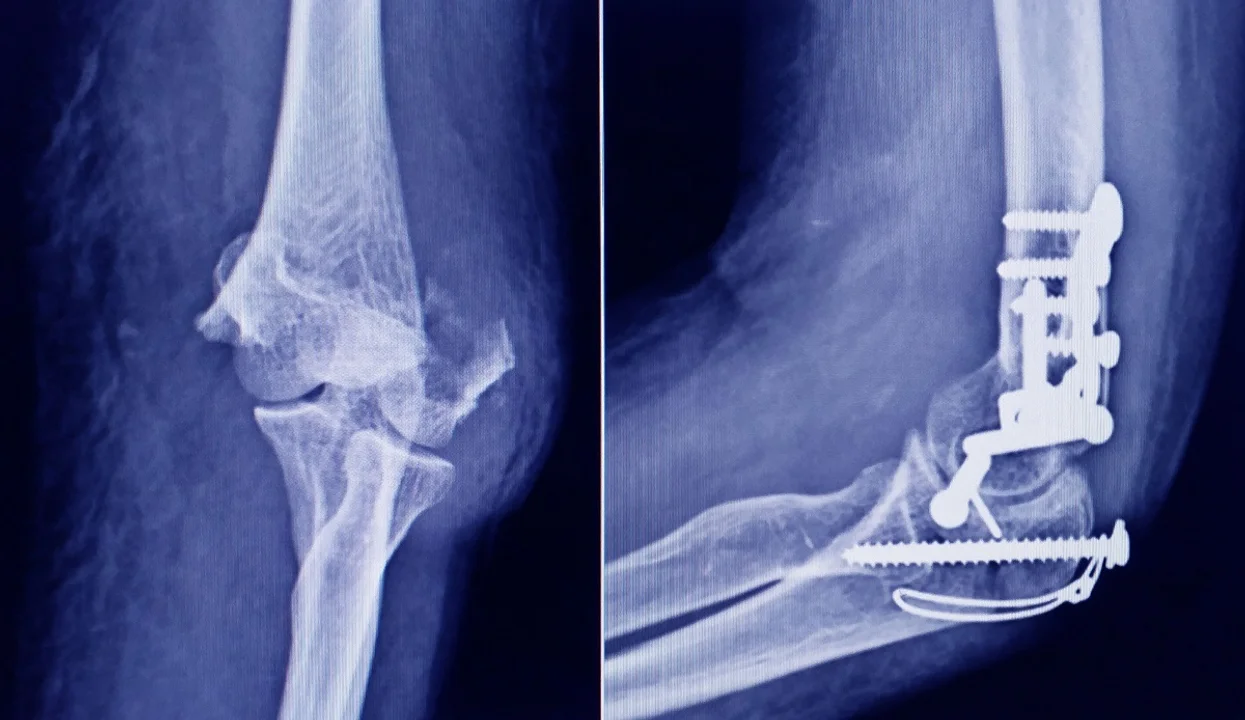
La ANMAT ordenó la prohibición del uso, comercialización y distribución en todo el territorio nacional de todos los lotes del tornillo traumatológico “SPIN® 2.0 – REF 112 013 – ND – MATERIAL Ti – INTEGRA – NEWDEAL SAS”, al constatar que el producto carece de registro sanitario en la Argentina y que se desconocen sus condiciones de seguridad y eficacia.
Un implante sin registro detectado en fiscalizaciones
La medida se formalizó mediante la Disposición Nº 1146/2026, tras una inspección en la que se halló una unidad del tornillo acondicionada en una bolsa termosellada, “sin datos del titular responsable en la Argentina ni información de registro sanitario”.
Se trata de un producto médico utilizado en cirugía traumatológica para la fijación de fragmentos óseos y procedimientos de osteosíntesis, por lo que su falta de trazabilidad y habilitación regulatoria supone un riesgo directo para los pacientes.

Tras las verificaciones en el Registro Nacional de Productores y Productos de Tecnología Médica (RPPTM), la ANMAT confirmó que el dispositivo no se encuentra inscripto, por lo que se trata de “un producto médico sin registro sanitario, del cual se desconocen sus características, funcionalidad y seguridad”.
Objetivo: proteger a pacientes y profesionales de la salud
En consecuencia, el organismo dispuso la prohibición del tornillo SPIN® 2.0 en todos sus lotes y presentaciones, “con el objetivo de proteger a pacientes y profesionales de la salud, garantizando que los productos médicos comercializados en el país cumplan con los estándares de seguridad, calidad y eficacia establecidos por la normativa vigente”.
La decisión refuerza el rol de la ANMAT en el control de dispositivos implantables de alto riesgo y marca una señal clara para toda la cadena de proveedores traumatológicos e importadores de tecnología médica en el mercado argentino.

Riesgos clínicos directos
- Fallas mecánicas: rotura del tornillo, aflojamiento o deformación por falta de controles de calidad, lo que puede llevar a pérdida de fijación ósea, retraso de consolidación o necesidad de reoperar.
- Infecciones: procesos de fabricación y esterilización no auditados aumentan el riesgo de contaminación microbiana y de infecciones profundas difíciles de tratar.
- Reacciones a materiales: si la aleación no es la declarada o no cumple normas ISO (biocompatibilidad, corrosión), puede producir inflamación local, alergias o liberación de partículas metálicas.
Riesgos de seguridad y trazabilidad
- Sin registro no hay evaluación de seguridad y eficacia por la autoridad sanitaria, ni verificación de rotulado, vida útil, lote o esterilidad.
- Ante un evento adverso, es muy difícil rastrear lote, fabricante real o distribuidor, lo que complica retirar productos similares y proteger a otros pacientes.
Riesgos legales y para el sistema de salud
- Para el cirujano y la institución, usar dispositivos no homologados expone a responsabilidad profesional y demandas, porque implica apartarse de la normativa.
- Para el sistema de salud, aumenta costos por complicaciones, reoperaciones y días extra de internación que podrían haberse evitado con tecnología validada.









Leave A Comment