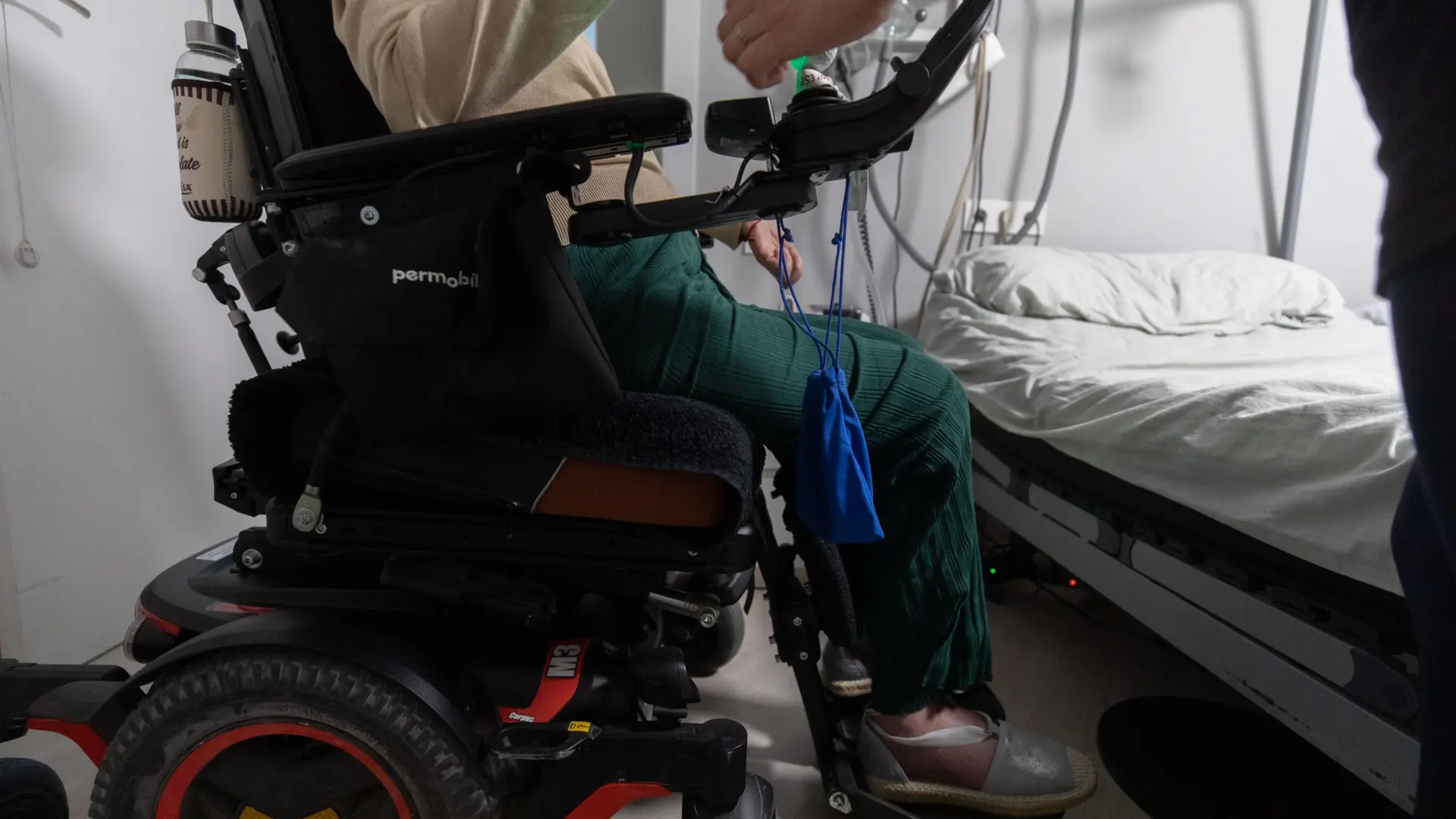
Fármaco español AP-2 para ELA: luz verde al primer ensayo en humanos de Molefy Pharma
- curecompass
- 20 marzo, 2026
- I+D, Medicina
- CIB‑CSIC, ELA, EMA, esclerosis lateral amiotrófica, España, Hospital Universitario de La Princesa, Molefy Pharma, Portada
- 0 Comments
La AEMPS autorizó el inicio del ensayo clínico de fase I de AP-2, un fármaco experimental contra la esclerosis lateral amiotrófica desarrollado en el CIB‑CSIC y promovido por Molefy Pharma, que arrancará en abril en el Hospital Universitario de La Princesa con 70 voluntarios sanos y el respaldo de la designación de medicamento huérfano otorgada por la EMA.
La investigación en esclerosis lateral amiotrófica (ELA) en España suma un hito que combina ciencia pública, capital biotecnológico y validación regulatoria europea.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) dio luz verde al primer ensayo en humanos de AP-2, un compuesto surgido en el Centro de Investigaciones Biológicas Margarita Salas (CIB‑CSIC) y desarrollado clínicamente por Molefy Pharma, spin‑off del Consejo Superior de Investigaciones Científicas.
El estudio, que comenzará en abril en la Unidad de Ensayos Clínicos del Hospital Universitario de La Princesa (Madrid), supone el paso desde años de trabajo en modelos celulares y animales a la evaluación formal en personas.
Fase I en La Princesa: seguridad y farmacocinética en 70 voluntarios
La fase I se iniciará con 70 voluntarios sanos y tendrá como objetivo principal evaluar la seguridad del fármaco y su farmacocinética: cómo se absorbe, distribuye, metaboliza y elimina en el organismo. El diseño contempla administrar AP-2 —formulado en cápsulas— y monitorizar efectos adversos, parámetros de seguridad y niveles plasmáticos del compuesto.
Según el plan clínico, si los resultados son favorables, el programa avanzará en enero de 2027 hacia una fase posterior en personas diagnosticadas de ELA, inicialmente una fase Ib centrada aún en seguridad y toxicidad, ya en pacientes. La iniciativa se enmarca en la actividad investigadora del Hospital de La Princesa y del Centro ELA del Hospital Zendal de Madrid, que se ha consolidado como referencia para esta patología neurodegenerativa.
Un mecanismo dirigido a TDP‑43: devolver la proteína a su lugar y función
AP-2 se diseñó para actuar sobre uno de los mecanismos más característicos de la ELA: la alteración de la proteína TDP‑43, patológicamente modificada en más del 97% de los pacientes. En condiciones normales, TDP‑43 reside en el núcleo de la célula, pero en la enfermedad “sale del núcleo de las células hacia el citoplasma. Una vez allí sufre modificaciones, se rompe y se fosforila, proceso que le lleva a formar agregados tóxicos”, explicó Ana Martínez, investigadora del CIB‑CSIC y líder del Grupo de Química Médica y Biológica Traslacional.
“El objetivo es devolver TDP‑43 a su estado funcional”, resume Martínez. Para lograrlo, el equipo diseñó una molécula capaz de inhibir la quinasa CK1, una enzima que altera TDP‑43 mediante fosforilación. En modelos celulares, “en pruebas en modelos celulares, observamos como TDP‑43 tendía a recuperarse, podía volver al núcleo y recuperar su función”.
Los resultados se replicaron en modelos animales transgénicos que expresan TDP‑43 alterada. “En modelos animales modificados genéticamente para expresar la proteína TDP‑43 también obtuvimos resultados prometedores. Aunque todavía es pronto, si se reprodujeran estos datos, el fármaco podría ralentizar la enfermedad, e hipotéticamente frenarla”, destacó Carmen Gil, codirectora del grupo de investigación en el CIB‑CSIC.
Designación de medicamento huérfano: el aval de la EMA y el impulso de Molefy Pharma
El desarrollo de AP-2 recibió un impulso clave en octubre de 2025, cuando la Agencia Europea del Medicamento (EMA) le otorgó la designación de medicamento huérfano, figura reservada a tratamientos dirigidos a enfermedades raras o con escaso interés comercial. Esta etiqueta reconoce su potencial terapéutico y facilita el desarrollo clínico, con incentivos regulatorios y de mercado dentro de la Unión Europea.
La financiación y el empuje empresarial corren por cuenta de Molefy Pharma, biotecnológica surgida como spin‑off del CSIC y participada mayoritariamente por el grupo tecnológico ARQUIMEA. “Esta designación se otorga a medicamentos con potencial para tratar enfermedades raras y graves en la Unión Europea, cuando aportan un beneficio significativo frente a las escasas o inexistentes opciones disponibles”, subrayó la compañía al anunciar el reconocimiento de la EMA.
“El reconocimiento de la EMA a una compañía española subraya el talento científico del país y la capacidad de ejecutar desarrollo clínico competitivo a escala europea. Desde ARQUIMEA seguiremos apoyando a Molefy Pharma para convertir esta designación en resultados reales para los pacientes”, afirmó Diego Fernández, presidente de ARQUIMEA.
Una necesidad urgente: 4.000–4.500 personas con ELA y un solo fármaco aprobado
La ELA es una enfermedad neurodegenerativa sin cura que provoca la pérdida progresiva de las funciones motoras, afectando a la movilidad, el habla, la alimentación y la respiración. En España se estima que entre 4.000 y 4.500 personas conviven con esta patología, con alrededor de 1.000 nuevos diagnósticos al año, y una esperanza de vida tras el diagnóstico que oscila entre cinco y seis años.
En el plano farmacológico, el margen de maniobra sigue siendo muy limitado. Actualmente, el único tratamiento aprobado en Europa de uso generalizado es el riluzol, un fármaco con efecto paliativo que puede prolongar la supervivencia apenas unos meses. Se estima que el riluzol “puede prolongar la vida entre 6 y 19 meses” o, según otros análisis, entre 3 y 6 meses, lo que lo mantiene como herramienta esencial pero insuficiente frente a una enfermedad devastadora.
En este contexto, el inicio del ensayo clínico de AP‑2 representa “un avance relevante en la búsqueda de nuevas terapias capaces de modificar el curso de la enfermedad”, al apuntar a un mecanismo central compartido por la gran mayoría de los pacientes.
De los tubos de ensayo al mercado: qué se juega la biotecnología española
La autorización de la AEMPS no solo es un hito científico, sino también un test para el ecosistema de I+D biomédico español. El programa AP‑2 muestra cómo una molécula descubierta en laboratorios públicos (CIB‑CSIC), impulsada por una spin‑off como Molefy Pharma y acompañada por capital tecnológico de grupos como ARQUIMEA puede atravesar el umbral regulatorio y entrar en la competencia global por terapias modificadoras de enfermedad en ELA, un segmento donde la necesidad clínica es alta y la barrera de entrada científica sigue siendo considerable.
En un mercado donde, hasta ahora, el riluzol domina como fármaco de referencia con un beneficio modesto, y donde nuevos tratamientos aprobados por la EMA han tardado casi tres décadas en llegar, la evolución clínica de AP‑2 será observada de cerca por pacientes, neurólogos y la industria farmacéutica, que ve en los fármacos dirigidos a TDP‑43 una posible próxima generación de terapias para ELA y otras enfermedades neurodegenerativas vinculadas a esta proteína.









Leave A Comment