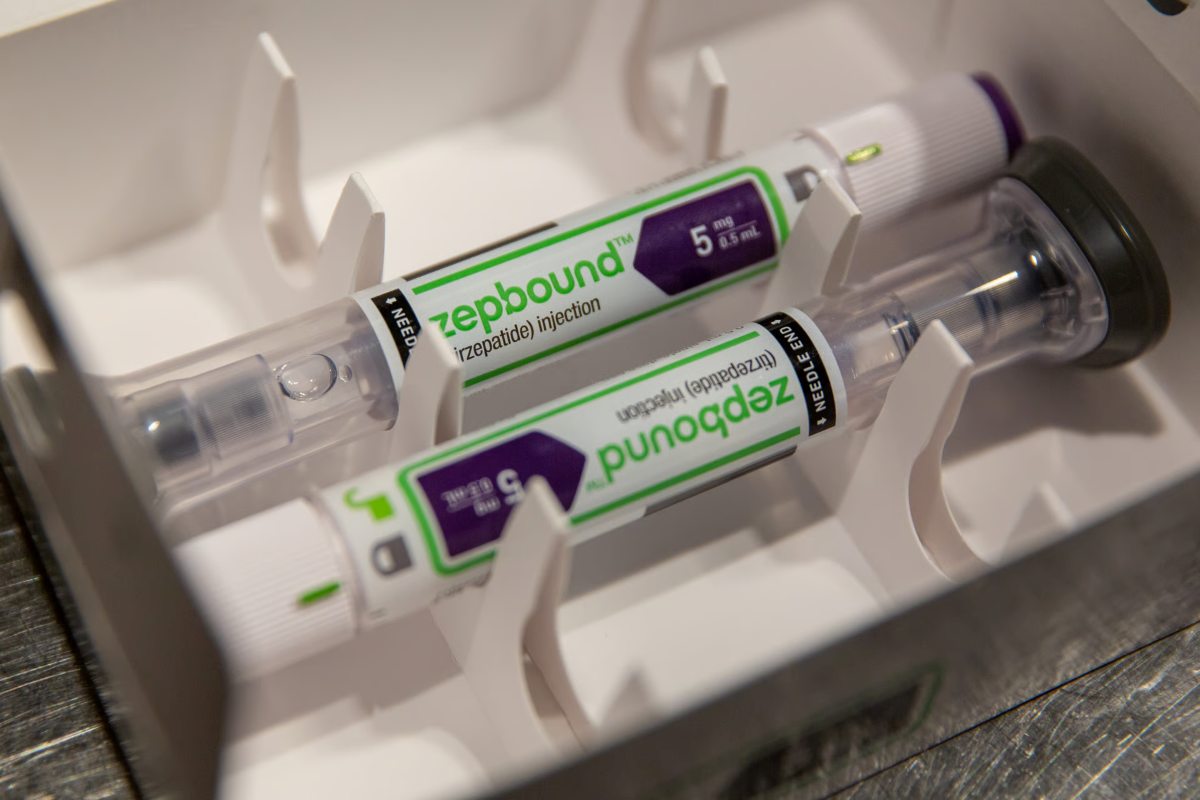
Alerta por riesgos para la salud: Eli Lilly detecta impureza en un medicamento para la obesidad
- curecompass
- 12 marzo, 2026
- Importante, Medicina
- B12, David Hyman, Eli Lilly, FDA, Mounjaro, Portada, tirzepatida, Zepbound
- 0 Comments
Eli Lilly advirtió públicamente que formulaciones magistrales para bajar de peso que combinan vitamina B12 con tirzepatida, el principio activo de su blockbuster Zepbound y del antidiabético Mounjaro, presentan “niveles significativos” de una impureza química de efectos desconocidos en humanos, tras analizar diez muestras de productos compuestos obtenidos en farmacias, medspas y redes de telemedicina en Estados Unidos.
Una impureza en todos los productos compuestos analizados
En una carta pública difundida este jueves, basada en pruebas de laboratorio sobre formulaciones comercializadas como versiones “compuestas” de tirzepatida, Lilly informó que detectó “niveles significativos de una impureza que resulta de una reacción química entre la tirzepatida y la vitamina B12” en los diez productos analizados. La empresa detalló que esa impureza fue identificada “en todas las diez muestras testeadas”, lo que descarta que se trate de un hallazgo aislado.
“No se sabe nada sobre sus efectos a corto o largo plazo en humanos, el impacto potencial en la interacción del fármaco con los receptores GLP-1 y GIP, la toxicidad, las reacciones inmunes o cómo se absorbe, distribuye, metaboliza y elimina”, advirtió la carta publicada en la web corporativa. Lilly notificó sus hallazgos a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y pidió un retiro a nivel nacional de los productos que contienen tirzepatida combinada con vitamina B12.
El comunicado es el último capítulo de la ofensiva legal y regulatoria del laboratorio contra farmacias de formulación, centros de bienestar y empresas de telemedicina que venden copias no autorizadas de Zepbound y Mounjaro.
Lilly ya ha presentado demandas por comercialización de productos que aseguran contener tirzepatida y que, según la compañía, se amparan indebidamente en una disposición estrecha de la ley federal que permite la formulación personalizada solo cuando el paciente necesita dosis o combinaciones no disponibles en los medicamentos aprobados.
“Los productos compuestos pueden ser riesgosos”: la advertencia de Lilly y la FDA
“La FDA advierte que los productos compuestos pueden ser riesgosos para los pacientes porque no se revisan en cuanto a seguridad, eficacia ni calidad. Añadir una sustancia reactiva como la vitamina B12 sin pruebas clínicas ni la revisión de la FDA conlleva riesgos adicionales desconocidos”, señaló David Hyman, director médico de Lilly, citado en la carta. El ejecutivo insistió en que estas formulaciones “bajo el paraguas de la personalización” en realidad incorporan “aditivos no testados” que crean “nuevos fármacos combinados, sin estudios clínicos ni evaluación regulatoria independiente”.
Lilly remarcó que “la mayoría de los vendedores ponen los mismos aditivos no probados en todas sus imitaciones de tirzepatida”, por lo que esos productos “no son personalizados en ningún sentido significativo”.
La compañía sostuvo que las versiones compuestas con B12 “puede suponer riesgos aún mayores para los pacientes de lo que se conocía anteriormente”, dado que, además de esta nueva impureza, sus análisis previos vienen detectando contaminación bacteriana, niveles elevados de endotoxinas y otras impurezas ausentes en sus medicamentos aprobados por FDA.
Telemedicina, GLP‑1 compuestos y un giro regulatorio más estricto
La advertencia de Lilly se produce en un contexto de mayor presión de la FDA sobre el mercado de GLP‑1 y agonistas afines. A comienzos de marzo, el organismo envió cartas de advertencia a 30 empresas de telemedicina por hacer “afirmaciones falsas o engañosas” sobre versiones compuestas de medicamentos para adelgazar, incluyendo sugerencias de equivalencia con productos aprobados y ocultamiento de su origen real detrás de marcas propias.
La agencia advirtió que los fármacos compuestos “no están aprobados por la FDA”, y por lo tanto no han sido evaluados en forma independiente en cuanto a seguridad, eficacia o calidad.
En febrero, la telemedicina Hims & Hers quedó bajo escrutinio por anunciar una píldora compuesta de semaglutida copia de Wegovy, lo que derivó en advertencias regulatorias y en un giro del negocio hacia la venta de productos originales de Novo Nordisk tras un acuerdo entre ambas compañías.
Ese caso, sumado a la nueva impureza detectada en formulaciones con tirzepatida y B12, refuerza un giro de “nueva era de cumplimiento” en torno a los GLP‑1, en la que big pharma, FDA y proveedores digitales de salud redefinen sus estrategias en un mercado de obesidad multimillonario donde la frontera entre innovación, acceso y seguridad está cada vez más vigilada,









Leave A Comment